西雅图的研究人员开发了一种技术,可以量化整个斑马鱼胚胎中因关键基因的特定编辑而发生的基因活性变化。该方法使得量化数千个胚胎发育过程中数百万个细胞的基因活性和遗传变异的影响成为可能。
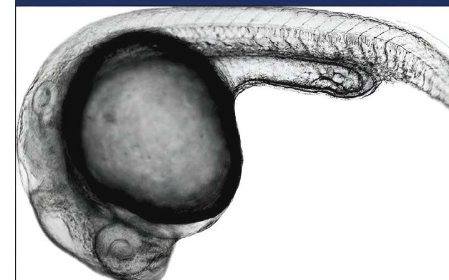
研究人员表示,这一进展将加速对正常胚胎发育的研究,并促进对特定基因突变如何影响整个胚胎细胞并导致疾病的理解。
“现在我们可以利用斑马鱼来确定特定基因的丢失如何影响生物体中的所有细胞,”德国EMBL海德堡的共同主要作者LaurenSaunders说。她最近是科尔·特拉普内尔(ColeTrapnell)实验室的博士后研究员,科尔·特拉普内尔是该研究的高级合著者。特拉普内尔是华盛顿大学医学院基因组科学副教授。现任FredHutch癌症中心研究员的SanjayR.Srivastan和华盛顿大学医学院生物化学名誉教授DavidKimelman分别是共同主要作者和共同高级作者。
桑德斯说:“这项研究提供了有关该基因的作用和位置的重要线索,并且也许有一天会展示不同的疗法如何预防或治疗相关的遗传性疾病。”
该研究结果于11月15日发表在《自然》杂志上,论文题为“单细胞分辨率下的胚胎规模反向遗传学”。
先前的研究绘制了斑马鱼胚胎细胞中基因表达差异的图谱,但这些图谱并未揭示个体胚胎之间基因表达的差异。早期的图谱也缺乏胚胎发生中后期阶段的紧密间隔的时间点。此外,过去的结果仅代表了该生物体野生型版本的基因表达谱,或仅在单个时间点的几个遗传扰动。
在这项新研究中,研究人员对1800多个胚胎的转录组进行了标记。然后,他们通过在胚胎发育过程中的19个时间点取样,追踪每种细胞类型随时间的变化。他们还引入了23种不同的遗传扰动,从而可以了解每种突变如何随着时间的推移影响生物体所有细胞类型的基因表达和细胞发育。
为了追踪哪些细胞来自哪些胚胎,研究人员使用了一种名为sci-Plex的技术,该技术是由特拉普内尔和威斯康星大学医学院基因组科学教授、布罗特曼巴蒂研究所科学主任JayShendure的实验室开发的。精准医学和霍华德休斯医学研究所研究员,他也是这项研究的共同作者。
通过这项技术,研究人员首先用短DNA分子标记每个胚胎的细胞核,每个胚胎都有独特的序列。这些序列充当条形码,使研究人员能够识别哪个细胞来自哪个胚胎。通过这种方法,他们分析了超过300万个细胞。
为了确定每种细胞类型中哪些基因处于活跃状态,他们利用了这样一个事实:当基因处于活跃状态时,其DNA中编码的遗传指令必须首先被复制到称为信使RNA或mRNA的相关分子中。然后细胞使用mRNA编码的指令作为蓝图来合成基因编码的蛋白质。当基因活跃时,其mRNA水平在细胞内升高;当它不活跃时,其mRNA水平较低或不存在。因此,mRNA水平可以告诉您基因何时“开启”或“关闭”。
由于每种细胞类型具有不同的功能和不同的基因表达特征,因此可以仅通过测量mRNA来识别哪些细胞代表不同的细胞类型。因此,研究人员不仅可以量化基因表达如何响应遗传扰动而变化,还可以量化胚胎中某些细胞群是否增加或减少。
桑德斯说,这些发现将扩大对正常和异常胚胎发育的认识,并增进对动物和人类进化的理解。
研究人员发现细胞的胚胎起源、最终结果和基因表达谱之间存在一些令人惊讶的关系。通过研究对脊索(一种贯穿胚胎长度的杆状结构)发育重要的基因,他们发现具有脊索样基因表达谱的细胞实际上是早期的颅底软骨。
“在斑马鱼和人类中,头骨有两个胚胎起源,”桑德斯说。“我们发现,成为颅骨底部的细胞类似于脊索的细胞,而不是包括面部在内的早期颅骨软骨的其余部分。目前还不清楚以前的种群是如何进化的,现在我们的数据使我们能够对脊椎动物进化过程中头骨软骨生成细胞如何产生提出新的假设。”
